Com morte de jovem sob investigação, Conass questiona Anvisa sobre vacinação de adolescentes
Estado de São Paulo registrou morte de jovem que tomou a vacina da Pfizer, mas afirma que caso não tem relação com o imunizante
atualizado
Compartilhar notícia
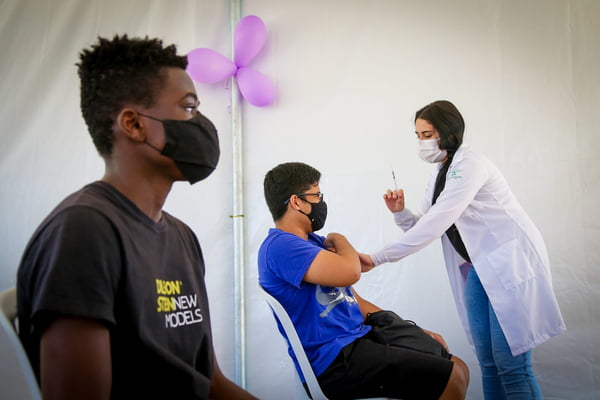
O Conselho Nacional de Secretários Estaduais de Saúde (Conass) enviou, nesta quinta-feira (16/9), um ofício à Agência Nacional de Vigilância Sanitária (Anvisa) questionando a continuidade da imunização de adolescentes contra a Covid-19, com administração da vacina da Pfizer.
O documento foi enviado após o Ministério da Saúde publicar, nesta manhã, uma nota técnica recomendando a suspensão da imunização de jovens de 12 a 17 anos.
Segundo o Conass, o governo federal recebeu a notificação de um “possível efeito adverso grave à vacina da Pfizer em adolescente do estado de São Paulo”. A pasta, no entanto, ainda não se posicionou sobre o caso.
Em nota, o governo de São Paulo confirmou o óbito do jovem, mas disse que a morte não tem ligação com o imunizante da Pfizer. O caso ocorreu em São Bernardo do Campo, município paulista.
“Até o momento, não há comprovação de relação da vacina ao óbito de um jovem de São Bernardo do Campo. O Centro de Vigilância Epidemiológica do Estado de São Paulo está investigando o caso devido à relação temporal com a aplicação da vacina. Qualquer afirmação ainda é precoce e temerária”, ressaltou o estado.
Além disso, o governo local considerou “irresponsável” o compartilhamento de informações sobre a morte do jovem. “É irresponsável a disseminação de qualquer informação que traga medo e insegurança aos adolescentes e familiares”, divulgou o estado, em nota.
Em nota, a Prefeitura de São Bernardo do Campo comunicou que o jovem tinha 16 anos de idade e estava internado no Hospital e Maternidade Vida’s. O órgão disse que, assim que soube do caso, “realizou, prontamente, a notificação do caso à Vigilância Epidemiológica do Estado de São Paulo para as devidas investigações”.
“Não há, até o momento, qualquer comprovação que relacione a vacinação da adolescente com sua morte. O município segue a diretriz do Plano Estadual de Imunização (PEI) e, desde 16 de agosto, realiza a aplicação da vacina contra o coronavírus no público adolescente (12 a 17 anos), com o imunizante da Pfizer”, informou a prefeitura, em nota.
A reportagem procurou o Ministério da Saúde e a Anvisa para se manifestarem sobre o assunto, mas não obteve retorno até a publicação deste texto. O espaço segue em aberto.
 ***vacinação-covid-adolescente
***vacinação-covid-adolescente
A miocardite é mais comum entre os jovens, observada com maior frequência entre os meninos após a segunda dose. Ela pode causar dor no peito e batimentos cardíacos acelerados, sintomas que desaparecem em poucos dias Igo Estrela/Metrópoles
 Começa a vacinação contra a Covid-19 para adolescentes com 17 anos. ( UBS 1 do Núcleo Bandeirante )
Começa a vacinação contra a Covid-19 para adolescentes com 17 anos. ( UBS 1 do Núcleo Bandeirante )
Cai o número de óbitos Igo Estrela/Metrópoles
 Começa a vacinação contra a Covid-19 para adolescentes com 17 anos. ( UBS 1 do Núcleo Bandeirante )
Começa a vacinação contra a Covid-19 para adolescentes com 17 anos. ( UBS 1 do Núcleo Bandeirante )
Vacina contra a Covid-19 Igo Estrela/Metrópoles
 Começa a vacinação contra a Covid-19 para adolescentes com 17 anos. ( UBS 1 do Núcleo Bandeirante )
Começa a vacinação contra a Covid-19 para adolescentes com 17 anos. ( UBS 1 do Núcleo Bandeirante )
Vacina contra a Covid-19 Igo Estrela/Metrópoles
A página oficial da Anvisa informa que, ao registrar qualquer efeito adverso após a vacinação, a autoridade de saúde deve acessar o sistema eletrônico VigiMed e notificar a suspeita do caso.
As notificações são analisadas pelos técnicos da Anvisa de acordo com a gravidade, risco associado ao evento adverso e previsibilidade. Em situações mais graves, o registro pode resultar na abertura de um processo de investigação.
Durante a apuração, a Anvisa toma diversas medidas: “desde a comunicação do risco sanitário, a partir da elaboração e posterior divulgação de alertas e informes, bem como alteração de bula, restrição de uso ou de comercialização, interdição de lotes e até mesmo o cancelamento do registro sanitário do medicamento ou da vacina”, conforme consta na página oficial da agência.
“Prioridades”
Antes do evento adverso, o Conass pressionou o Ministério da Saúde para favorecer grupos prioritários.
Na segunda-feira (13/9), a entidade enviou um ofício ao ministro da Saúde, Marcelo Queiroga, pedindo que o governo federal priorizasse a aplicação da dose de reforço do imunizantecontra a Covid-19 em idosos acima dos 60 anos e imunossuprimidos.
Atualmente, o Ministério da Saúde prevê a dose de reforço apenas para quem tem mais de 70 anos. O Conass também pede que o Ministério da Saúde priorize a aplicação da dose de reforço naqueles que estão em lares de longa permanência.
O documento ainda solicita que, com o atraso da AstraZeneca para a segunda dose, o Programa Nacional de Imunização (PNI) suspenda a aplicação em adolescentes sem comorbidades enquanto os grupos prioritários não forem revacinados.
A entidade usa como argumento a falta de doses da AstraZeneca para a segunda aplicação. Alguns estados começaram a aplicar a Pfizer em quem precisava tomar uma segunda dose da AstraZeneca e estava com o esquema vacinal atrasado.
Neste momento, a fórmula da Pfizer é a única aprovada pela Anvisa para a faixa entre 12 e 17 anos no Brasil.
Suspensão
Inicialmente, o governo federal pretendia vacinar 20 milhões de pessoas de 12 a 17 anos com o imunizante da Pfizer.
Em nota técnica enviada às secretarias de Saúde, a pasta informa que “revisou” a recomendação. Como justificativa, o ministério mencionou que a maioria dos adolescentes sem comorbidades acometidos pela Covid-19 demonstra evolução “benigna” e permanece assintomática.
525651294 Nota Informativa Do Ministerio Da Saude Sobre Vacinacao Em Adolescentes Contra a Covid 19 by Rebeca Borges on Scribd
A nota foi publicada no sistema do Ministério da Saúde às 21h30 de quarta-feira (16/9), ou seja, menos de 24 horas após o início da campanha para esse público.
Segundo a secretária Extraordinária de Atenção à Covid-19, Rosana Leite de Melo, a Organização Mundial de Saúde (OMS) não recomenda a imunização de crianças e adolescentes, com ou sem comorbidades.